Fouzia Boulmedais, physico-chimiste, a développé l’idée de créer des pansements connectés. L’objectif : révolutionner la prise en charge de patients diabétiques ou grands brûlés. Avec Anne Hébraud, elles développent ce concept à l’Institut Charles Sadron à Strasbourg, dans les laboratoires du CNRS.
« J’avais lu un article du professeur Messersmith. Il avait extrait des protéines que les moules sécrétaient, car il se demandait comment elles arrivaient à se coller aux coques de bateaux » explique Fouzia Boulmedais. Pour elles, les moules sont le parfait exemple de ce qui devrait être fait dans la médecine : coller les pansements le plus rapidement possible et de façon à ce qu’il soit solidement accroché. « Le but, c’est de mettre une électrode, une languette qui se collerait sur un pansement souple. Cette languette capterait ce qu’il y a dans la plaie.», complète Fouzia Boulmedais Rapidement, l’idée commence à naître : la L-Dopa sécrétée présente la faculté de se coller aux métaux, mais aussi aux matières organiques. Sachant que certains enzymes sont déjà capables de communiquer des informations sur des plaies, notamment le glucose dans le cas des personnes diabétiques, elle développe le projet de créer des pansements connectes pouvant communiquer des informations sur les plaies qui se cachent en dessous.
Utilité future
Dans le cas de plaies chroniques, cela peut prendre un long moment avant de se refermer ce qui nécessite des soins réguliers. « C’est compliqué pour les patients, mais aussi pour les infirmières » explique Fouzia Boulmedais. Sans compter le trajet quotidien, le pansement est changé tous les jours, car il est encore impossible de savoir ce qu’il se trouve sous la plaie, le changement de ce pansement représente aussi un risque d’infection bactérienne. « Le pansement connecté réduirait fortement les coûts dans le domaine de la santé : les infirmières n’auraient plus à se déplacer tous les jours » souligne Fouzia Boulmedais. Cette technologie permettrait aussi d’identifier plus rapidement le moindre problème pouvant se cacher sous la membrane.

Encore un long chemin
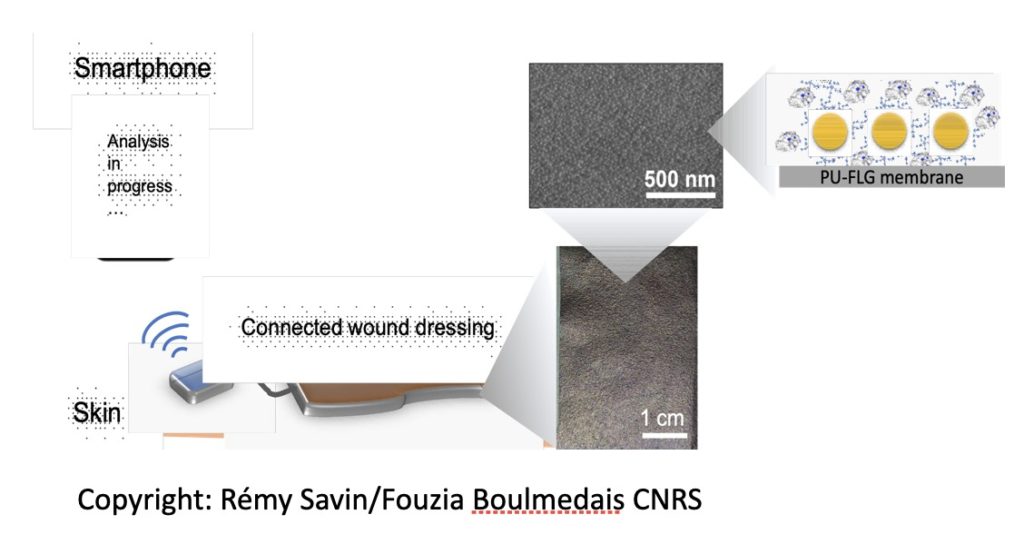
À l’heure actuelle, les recherches se poursuivent au sein des locaux de l’Institut Charles Sadron. « On est encore sur la preuve de concept », explique la physico-chimiste. En effet, bien que les recherches aient déjà beaucoup avancé, il reste un long chemin jusqu’à la commercialisation du pansement. La membrane qui constituera le pansement est déjà prête. Anne Hebraud l’a crée de façon à ce qu’il y ait trois couches à l’intérieur : une première en contact avec la plaie, une deuxième qui a pour rôle de lire les informations et la troisième qui les transmet. La membrane reste poreuse bien que ses pores sont extrêmement petits et peuvent aller jusqu’à une taille A4. L’alliage des enzymes et des fibres présents permet une transmission électrique d’information ce qui pourrait très facilement communiquer des informations sur le glucose présent dans une plaie, l’acide urique, mais aussi le pH, indicateur d’infection. Aucune date de lancement n’est encore prévue« Maintenant, il va falloir trouver des partenaires pour développer l’interface », car les pansements devraient pouvoir communiquer des informations via Bluetooth.